

DOI: 10.26820/recimundo/4.(3).julio.2020.230-241
URL:http://recimundo.com/index.php/es/article/view/866
EDITORIAL: Saberes del Conocimiento
Revista: RECIMUNDO
ISSN: 2588-073X
Tipo de Investigación: Artículo de Revisión
Código UNESCO: 3205 Medicina Interna
Paginas: 230-241

Dionisia Emilia Sánchez Núñez1; Mirian Isabel Hernandez Castro2; Gema Elizabeth Saltos Bazurto3; Jessica Yahaira Barberan Castro4
 https://orcid.org/0000-0002-4418-8418
https://orcid.org/0000-0002-4418-8418 https://orcid.org/0000-0001-5306-871X
https://orcid.org/0000-0001-5306-871X https://orcid.org/0000-0002-2188-5296
https://orcid.org/0000-0002-2188-5296 https://orcid.org/0000-0001-7767-7421
https://orcid.org/0000-0001-7767-7421CORRESPONDENCIA
Dionisia Emilia Sánchez Núñez
dionamapy@gmail.com
Portoviejo, Ecuador
La embolia pulmonar sigue siendo una causa de muerte común y potencialmente prevenible. Este artículo revisa la epidemiología, las características clínicas, el proceso de diagnóstico y el tratamiento de la embolia pulmonar. Los factores de riesgo bien reconocidos incluyen hospitalización reciente, otras causas de inmovilización, cáncer y exposición a estrógenos. Se han desarrollado algoritmos de diagnóstico para la embolia pulmonar que incorporan la evaluación de la probabilidad previa a la prueba y la prueba del dímero D para limitar la necesidad de imágenes de diagnóstico. La anticoagulación debe administrarse con prontitud a todos los pacientes con embolia pulmonar, siendo la heparina de bajo peso molecular el anticoagulante inicial de elección, aunque la trombólisis está indicada para pacientes que presentan compromiso hemodinámico. Después de la anticoagulación inicial, la terapia con Warfarina debe continuarse durante un mínimo de 3 meses. Se debe considerar la anticoagulación a largo plazo con Warfarina en pacientes con embolia pulmonar no provocada, debido a un mayor riesgo de recurrencia después de suspender la anticoagulación. Es probable que la disponibilidad de nuevos anticoagulantes tenga un impacto significativo en el tratamiento de los pacientes con embolia pulmonar, aunque aún no se ha definido el papel exacto de estos fármacos.
Palabras claves: Embolia pulmonar; factores de riesgo; productos de degradación de fibrina fibrinógeno.
Pulmonary embolism remains a common and potentially preventable cause of death. This article reviews the epidemiology, clinical features, diagnostic process, and treatment of pulmonary embolism. Well recognized risk factors include recent hospitalization, other causes of immobilization, cancer, and estrogen exposure. Diagnostic algorithms for pulmonary embolism that incorporate assessment of pretest probability and D-dimer testing have been developed to limit the need for diagnostic imaging. Anticoagulation should be administered promptly to all patients with pulmonary embolism with low molecular weight heparin being the initial anticoagulant of choice, although thrombolysis is indicated for patients presenting with hemodynamic compromise. Following initial anticoagulation warfarin therapy should be continued for a minimum of 3 months. Long term anticoagulation with warfarin should be considered in patients with unprovoked pulmonary embolism, due to an increased risk of recurrence after ceasing anticoagulation. The availability of new anticoagulants is likely to significantly impact on the treatment of patients with pulmonary embolism, although the exact role of these drugs is still to be defined.
Keywords: Pulmonary embolism; risk factors; fibrinfibrinogen degradation products.
A embolia pulmonar continua sendo uma causa de morte comum e potencialmente evitável. Este artigo revisa a epidemiologia, características clínicas, processo diagnóstico e tratamento da embolia pulmonar. Fatores de risco bem reconhecidos incluem hospitalização recente, outras causas de imobilização, câncer e exposição ao estrogênio. Algoritmos de diagnóstico para embolia pulmonar que incorporam avaliação de probabilidade pré-teste e teste de dímero D foram desenvolvidos para limitar a necessidade de diagnóstico por imagem. A anticoagulação deve ser administrada imediatamente a todos os pacientes com embolia pulmonar, sendo a heparina de baixo peso molecular o anticoagulante inicial de escolha, embora a trombólise seja indicada para pacientes com comprometimento hemodinâmico. Após a anticoagulação inicial, a terapia com varfarina deve ser continuada por um período mínimo de 3 meses. A anticoagulação de longo prazo com varfarina deve ser considerada em pacientes com embolia pulmonar não provocada, devido a um risco aumentado de recorrência após a interrupção da anticoagulação. É provável que a disponibilidade de novos anticoagulantes tenha impacto significativo no tratamento de pacientes com embolia pulmonar, embora o papel exato desses medicamentos ainda não esteja definido.
Palavras-chave: Embolia pulmonar; fatores de risco; produtos de degradação de fibrinfibrinogênio.
INTRODUCCIÓN
En 1868, Trousseau identificó por primera vez una estrecha conexión entre la tromboembolia venosa (TEV) y el cáncer (Blom, Doggen, & Osanto, 2015). Muchos estudios recientes han demostrado que la TEV se asocia con peores resultados en pacientes con cáncer y que la TEV es la segunda causa principal de muerte después del cáncer entre los pacientes con cáncer. La TEV incluye trombosis venosa profunda (TVP) y embolia pulmonar (EP); el primero a menudo conduce a un síndrome postrombótico y el segundo a menudo da como resultado complicaciones más peligrosas, como infarto pulmonar e hipertensión pulmonar tromboembólica crónica. Según un estudio anterior, el cáncer de pulmón (CP) es la neoplasia maligna más comúnmente asociada con la EP. Además, múltiples estudios clínicos han confirmado que la aparición de EP está asociada con una mayor tasa de muerte entre los pacientes con CL (Chuang & Yu, 2016), que representa el 10% de las muertes. Sin embargo, entre los pacientes con CL con EP que reciben terapia de anticoagulación temprana, la tasa de mortalidad se reduce cuatro veces en comparación con la de los pacientes que no reciben terapia temprana.
Por tanto, la identificación, el diagnóstico y el tratamiento precoz de la EP podría reducir la mortalidad entre los pacientes con CP, de hecho, el diagnóstico erróneo o el diagnóstico perdido de la EP a menudo ocurre en un entorno clínico porque los síntomas clínicos de la EP generalmente no son fácilmente reconocibles. Según un estudio retrospectivo, la fatiga y la dificultad para respirar son los síntomas más comunes entre los pacientes con cáncer con EP insospechada, lo que a menudo no se considera una posible explicación. Por tanto, es importante investigar las características clínicas asociadas con la EP entre los pacientes con CL.
Revisiones sistemáticas anteriores han descrito la asociación entre CP y EP y han resumido las características clínicas relevantes de la EP en pacientes con CP. Por ejemplo, (Malgor, Bilfinger, & Labropoulos, 2012) describió que, entre los pacientes con CP con adenocarcinoma, la quimioterapia parece estar asociada con una EP más frecuente.
Los autores (Li, Wang, Ning, & Chen, 2018) no solo descubrieron la incidencia, las consideraciones fisiopatológicas, el tratamiento y la importancia pronóstica de la EP entre los pacientes con CP, sino que también resumieron los factores de riesgo asociados con la EP y mostraron que el adenocarcinoma, estadio TNM más avanzado, anemia, obesidad, antecedentes de enfermedad pulmonar obstructiva crónica (EPOC ), TVP, hospitalización en los 12 meses anteriores al diagnóstico de CL, cirugía, quimioterapia, fármacos dirigidos, catéter venoso central (CVC) y hemoglobina (Hb), glóbulos blancos (WBC), dímero D (DD), presión parcial de oxígeno (PaO2) y los niveles de antígeno carcinoembrionario (CEA) se asociaron con PE en pacientes con CL.
Este proceso permite a los médicos elegir el siguiente paso óptimo para determinar qué pruebas de imagen o de laboratorio se deben realizar, si corresponde. Para los IPE confirmados, el plan de manejo omite el paso de diagnóstico de EP y comienza con la evaluación clínica del paciente, solicitando pruebas cuando sea necesario, incluida la ecografía Doppler, la ecocardiografía y la reserva respiratoria. Luego se diseña el plan de tratamiento, que incluye medicamentos, admisión o alta, y cualquier procedimiento de intervención necesario, como el filtro de la vena cava inferior (VCI) o la trombólisis.
La complejidad de la EIP se debe a las múltiples posibilidades de tratamiento y, a menudo, se complica aún más por múltiples comorbilidades de alto riesgo (Key, Khorana, & Kuderer, 2020). Se han observado tasas similares de TEV recurrente, hemorragia mayor y mortalidad en pacientes con EIP en comparación con la EP sintomática y la mayoría de los EP mortales tienden a ser clínicamente insospechados. Además, el uso recomendado de anticoagulantes varía entre estudios o guías. Por ejemplo, el American College of Chest Physicians recomienda la observación de pacientes de bajo riesgo con EP subsegmentaria (con mayor confianza cuando la EP es incidental y aislada) y una ecografía bilateral normal de las piernas, mientras que la Sociedad Estadounidense de Oncología Clínica recomienda el tratamiento subsegmental incidental PE caso por caso (Key, Khorana, & Kuderer, 2020).
En el estudio de casos y controles actual, busca identificar características clínicas importantes y describir el manejo y los resultados de la EIP en pacientes con cáncer.
Metodología
Para el desarrollo de este proceso investigativo, se plantea como metodología la encaminada hacia una orientación científica particular que se encuentra determinada por la necesidad de indagar en forma precisa y coherente una situación, en tal sentido (Davila, 2015) define la metodología “como aquellos pasos previos que son seleccionados por el investigador para lograr resultados favorables que le ayuden a plantear nuevas ideas”.(p.66)
Lo citado por el autor, lleva a entender que el desarrollo de la acción investigativa busca simplemente coordinar acciones enmarcadas en una revisión bibliográfica con el fin de complementar ideas previas relacionadas a las Características clínicas en pacientes con cuadro de embolia pulmonar a través de una revisión de literatura, para así finalmente elaborar un cuerpo de consideraciones generales que ayuden a ampliar el interés propuesto.
Tipo de Investigación
Dentro de toda práctica investigativa, se precisan acciones de carácter metodológico mediante las cuales, se logra conocer y proyectar los eventos posibles que la determinan, así como las características que hacen del acto científico un proceso interactivo ajustado a una realidad posible de ser interpretada. En este sentido, se puede decir, que la presente investigación corresponde al tipo documental, definido por Castro (2016), “se ocupa del estudio de problemas planteados a nivel teórico, la información requerida para abordarlos se encuentra básicamente en materiales impresos, audiovisuales y /o electrónicos”. (p.41).
En consideración a esta definición, la orientación metodológicapermitió la oportunidad de cumplir con una serie de actividades inherentes a la revisión y lectura de diversos documentos donde se encontraron ideas explicitas relacionadas con los tópicos encargados de identificar a cada característica insertada en el estudio. Por lo tanto, se realizaron continuas interpretaciones con el claro propósito de revisar aquellas apreciaciones o investigaciones propuestas por diferentes investigadores relacionadas con el tema de interés, para luego dar la respectiva argumentación a los planteamientos, en función a las necesidades encontradas en la indagación.
Fuentes Documentales
El análisis correspondiente a las características que predomina en el tema seleccionado, llevan a incluir diferentes fuentes documentales encargadas de darle el respectivo apoyo y en ese sentido cumplir con la valoración de los hechos a fin de generar nuevos criterios que sirven de referencia a otros procesos investigativos. Para (CASTRO, 2016) las fuentes documentales incorporadas en la investigación documental o bibliográfica, “representa la suma de materiales sistemáticos que son revisados en forma rigurosa y profunda para llegar a un análisis del fenómeno.(p.41). Por lo tanto, se procedió a cumplir con la realización de una lectura previa determinada para encontrar aquellos aspectos estrechamente vinculados con el tema, con el fin de explicar mediante un desarrollo las respectivas apreciaciones generales de importancia.
Técnicas para la Recolección de la Información
La conducción de la investigación para ser realizada en función a las particularidades que determinan a los estudios documentales, tiene como fin el desarrollo de un conjunto de acciones encargadas de llevar a la selección de técnicas estrechamente vinculadas con las características del estudio. En tal sentido, (Bolívar, 2015), refiere, que es “una técnica particular para aportar ayuda a los procedimientos de selección de las ideas primarias y secundarias”. (p. 71).
Por ello, se procedió a la utilización del subrayado, resúmenes, fichaje, como parte básica para la revisión y selección de los documentos que presentan el contenido teórico. Es decir, que mediante la aplicación de estas técnicas se pudo llegar a recoger informaciones en cuanto a la revisión bibliográfica de los diversos elementos encargados de orientar el proceso de investigación. Tal como lo expresa, (Bolívar, 2015) “las técnicas documentales proporcionan las herramientas esenciales y determinantes para responder a los objetivos formulados y llegar a resultados efectivos” (p. 58). Es decir, para responder con eficiencia a las necesidades investigativas, se introdujeron como técnica de recolección el método inductivo, que hizo posible llevar a cabo una valoración de los hechos de forma particular para llegar a la explicación desde una visión general.
Asimismo, se emplearon las técnicas de análisis de información para la realización de la investigación que fue ejecutada bajo la dinámica de aplicar diversos elementos encargados de determinar el camino a recorrer por el estudio, según, (Bolívar, 2015) las técnicas de procesamiento de datos en los estudios documentales “son las encargadas de ofrecer al investigador la visión o pasos que debe cumplir durante su ejercicio, cada una de ellas debe estar en correspondencia con el nivel a emplear” (p. 123). Esto indica, que para llevar a cabo el procesamiento de los datos obtenidos una vez aplicado las técnicas seleccionadas, tales como: fichas de resumen, textual, registros descriptivos entre otros, los mismos se deben ajustar al nivel que ha sido seleccionado.
Resultados
Más de 150 años después de la primera descripción de Virchow de su tríada de factores de riesgo de tromboembolismo venoso (TEV), la embolia pulmonar (EP) sigue siendo una importante causa evitable de morbilidad y mortalidad. Tanto el diagnóstico como el tratamiento inicial de la EP todavía se realizan en gran medida en el ámbito hospitalario. Sin embargo, la comprensión y el conocimiento de la EP por parte del médico de atención primaria sigue siendo importante, debido a la necesidad de una alta sospecha diagnóstica de EP para permitir el reconocimiento rápido de una enfermedad potencialmente mortal y también a la creciente tendencia al alta temprana de los pacientes en tratamiento por EP.
Epidemiología
El tromboembolismo venoso, que consiste tanto en trombosis venosa profunda (TVP) como en EP, tiene una incidencia anual en poblaciones caucásicas de aproximadamente 1,5 por 1000con la incidencia aumentando con la edad. Aproximadamente 30 a 40% de los pacientes con TEV presentarán EP sintomática. (White, 2013)
La embolia pulmonar será mortal en hasta el 25% de los pacientes en los que se ha realizado el diagnóstico si no se trata con anticoagulación reduciendo sustancialmente el riesgo de EP fatal durante el período de tratamiento inicial a menos del 2%. Sin embargo, hasta en un 25% de las personas con EP, la presentación inicial será la muerte súbita antes de que se pueda iniciar la terapia (Heit, 2015). El riesgo de muerte en pacientes con EP confirmada que han sido tratados con anticoagulación a los 3 meses después del diagnóstico es aproximadamente del 10 al 15% siendo la mayoría debida a condiciones comórbidas.
Factores de riesgo de embolia pulmonar
Hay una serie de factores de riesgo bien definidos para la EP (tabla 1), cuya presencia elevará el nivel de sospecha diagnóstica en pacientes con síntomas sugestivos.
Hospitalización reciente
La trombosis venosa que ocurre después de una hospitalización reciente representa aproximadamente el 50% de los casos, con ingresos quirúrgicos y médicos recientes que representan una proporción igual de eventos. Hay un aumento de aproximadamente setenta veces en el riesgo de TEV después de una cirugía hospitalaria y un aumento de diez veces en el riesgo después de una cirugía ambulatoria, a pesar de la práctica quirúrgica moderna. El riesgo es máximo en 3 semanas después de la cirugía y permanece elevado hasta 12 semanas. Por tanto, la mayoría de los casos de EP relacionados con la cirugía se producirán tras el alta hospitalaria.
Tabla 1. Factores de riesgos de trombosis venosa
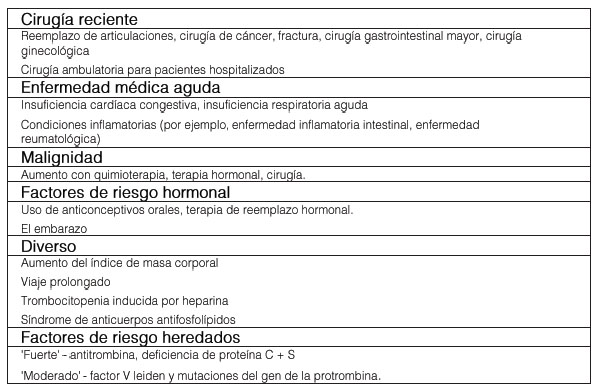
Fuente: (Heit, 2015)
Cáncer
Los pacientes con cáncer constituyen el 15-20% de los pacientes con TEV. El riesgo de trombosis venosa en pacientes con cáncer aumenta con la administración de quimioterapia, terapia hormonal y procedimientos quirúrgicos. Los tumores malignos con un alto riesgo de trombosis venosa incluyen cerebro, ovario y cáncer de páncreas (Lee, 2014).
Uso de píldoras anticonceptivas orales y embarazo
El uso de preparaciones de anticonceptivos orales combinados disponibles en la actualidad está asociado con un aumento de 2-7 veces en el riesgo de TEV. La magnitud del aumento del riesgo varía según el tipo de progesterona, siendo menor con las preparaciones de segunda generación (aumento de 2 a 4 veces en el riesgo) y mayor con píldoras de tercera generación o preparaciones que contienen ciproterona o drospirenona (aumento de 4 a 7 veces en riesgo) (Lidegaard, Løkkegaard, Svendsen, & Agger, 2016). Debido a la baja incidencia anual de fondo de TEV en mujeres en edad reproductiva (~ 1 de cada 10000), el riesgo absoluto en usuarias de anticonceptivos orales sigue siendo bajo, inferior al 0,1% anual.
La incidencia de TEV durante el embarazo y el período posparto es de aproximadamente 1 en 1000, es decir. aproximadamente diez veces mayor que en mujeres no embarazadas de edad similar. El riesgo de EP es mayor durante las 4 a 6 semanas posparto, con más del 50% de los episodios de EP relacionados con el embarazo durante este período (Simpson, Lawrenson, & Nightingale, 2011).
Viaje extendido
Se ha dado mucha publicidad al transporte aéreo como factor de riesgo de TEV. Sin embargo, en un gran estudio de cohortes reciente, menos del 2% de las personas con trombosis venosa habían emprendido un vuelo prolongado dentro de8 semanas antes del diagnóstico (Schreijer, Cannegieter, & Doggen, 2018). Los vuelos de menos de 4 horas no parecen estar asociados con ningún aumento en el riesgo de trombosis venosa, con vuelos de entre cuatro y 8 horas de duración asociados con un aumento del doble en el riesgo de TEV, y vuelos de más de 12 horas con un aumento del riesgo de cinco veces.Por tanto, la magnitud del aumento del riesgo es sustancialmente menor que la asociada con la cirugía reciente. Si bien hay menos datos, el riesgo de trombosis venosa con viajes de la misma duración en otros modos de transporte, incluidos el automóvil y el ferrocarril, parece similar al asociado con el vuelo (Cannegieter, Doggen, van Houwelingen, & Rosendaal, 2016).
Otros factores de riesgo
Las afecciones médicas comórbidas que se ha demostrado que son factores de riesgo de embolia pulmonar incluyen insuficiencia cardíaca, insuficiencia respiratoria aguda o crónica, enfermedad reumatológica aguda, infección aguda, enfermedad inflamatoria intestinal y aumento del índice de masa corporal. Los datos recientes sugieren que fumar se asocia con un aumento de 1,5 veces en el riesgo de trombosis venosa (Stein, Willis, & De Mets, 1981)
Presentación clínica de embolia pulmonar
Por lo general, se sospecha de embolia pulmonar debido a una falta de aire o que empeora la respiración además de aparición de dolor agudo en el pecho. La disnea está presente en 70 a 80% de los pacientes con EP confirmada,con dolor torácico presente en el 60-70% de los casos. Entre el 10 y el 20% de los pacientes con EP confirmada informan hemoptisis (Stein & Henry, 2007). Los síntomas en la presentación varían según la ubicación del trombo; los pacientes con émbolos pulmonares más grandes tienen más probabilidades de presentar disnea aislada (25% de los casos) y aquellos con émbolos más periféricos que causan infarto pulmonar con dolor torácico pleurítico +/– hemoptisis (60% de los casos). casos). Entre el 5 y el 8% de los pacientes con EP que sobreviven lo suficiente para realizar una evaluación diagnóstica presentarán colapso circulatorio, definido por una presión arterial sistólica de <90 mmHg (Kucher, Rossi, De Rosa, & Goldhaber, 2016) Una proporción de estos pacientes no presentará síntomas de dolor torácico ni disnea.
Las características clínicas que han demostrado ser predictivas de la presencia de EP incluyen síntomas concurrentes de TVP, antecedentes de síncope, presencia de dolor torácico pleurítico, taquipnea y taquicardia. Sin embargo, la presencia o ausencia de un solo síntoma o signo no se puede utilizar para confirmar o refutar el diagnóstico. Este hecho, junto con las consecuencias de un diagnóstico perdido, significa que el umbral para iniciar una investigación adicional en pacientes que presentan síntomas asociados con la EP, particularmente en ausencia de una explicación alternativa, debe ser bajo.
Algoritmos de diagnóstico de embolia pulmonar
La incidencia de EP confirmada en pacientes sometidos a investigación se ha reducido con el tiempo a una cifra actual de aproximadamente el 20%. Dado que la mayoría de los pacientes no tendrán EP confirmada, se han desarrollado algoritmos de diagnóstico para excluir de forma segura la EP y limitar la necesidad de diagnóstico por imágenes.
Reglas de predicción clínica para la embolia pulmonar
Los médicos experimentados pueden estratificar con precisión la probabilidad de EP mediante una evaluación clínica no estructurada (Chunilal, Eikelboom, & Attia, 2013). Se han desarrollado reglas de predicción clínica para formalizar este proceso, y la evaluación de la probabilidad previa a la prueba se utiliza para guiar las pruebas de diagnóstico adicionales. La regla de predicción más utilizada para la EP es el puntaje de Wells, en el que los puntos se otorgan según la presencia o ausencia de factores de riesgo y los síntomas y signos de la EP (tabla 2) (Wells, Anderson, & Rodger, 2000). Una versión simplificada que clasifique a los pacientes como EP improbable (prevalencia de EP 12%) o EP probable (prevalencia de EP 47%) es óptima para ayudar a excluir EP sin diagnóstico por imágenes.
Prueba de dímero D
El dímero D, un producto de degradación de la fibrina reticulada, es una prueba muy sensible para TEV reciente.Se puede utilizar una prueba de dímero D negativa para ayudar a excluir la EP en pacientes con una baja probabilidad previa a la prueba. En pacientes clasificados como EP con poca probabilidad con una prueba de dímero D altamente sensible negativa, la probabilidad de EP es suficientemente baja (<1%) para excluir el diagnóstico sin más pruebas. En pacientes clasificados como PE probable, la prevalencia de PE en pacientes con un dímero D negativo todavía es ~ 10%. Por lo tanto, los pacientes de la última categoría deben proceder directamente a la obtención de imágenes de diagnóstico sin que se realice una prueba de dímero D.
Diagnóstico por imágenes de embolia pulmonar
La angiografía pulmonar por tomografía computarizada (CTPA) se ha convertido en la investigación radiológica más utilizada para la sospecha de EP. El CTPA multidetector moderno es muy sensible para la EP, y se ha demostrado que un solo estudio negativo excluye de manera segura la EP (Perrier, Roy, & Sanchez, 2015). Un defecto de llenado dentro de un vaso segmentario o más proximal confirma la EP y justifica el inicio del tratamiento. Un beneficio adicional de CTPA es que también se detectarán diagnósticos alternativos. Las desventajas incluyen la detección de pequeños émbolos subsegmentarios, para los cuales la necesidad de anticoagulación sigue sin estar clara, las complicaciones del contraste y las preocupaciones con respecto al grado de exposición a la radiación y el consiguiente aumento en el riesgo de cáncer de mama, particularmente en mujeres en edad reproductiva (Hurwitz, Reiman, & Yoshizumi, 2017)
La exploración de perfusión ventilatoria (VQ) sigue siendo un método alternativo de obtención de imágenes para la EP, en particular en individuos sin enfermedad pulmonar preexistente en quienes la incidencia de resultados no diagnósticos disminuye.Tiene la ventaja sobre la CTPA de no requerir exposición al contraste y, por lo tanto, es la investigación de elección en pacientes con insuficiencia renal. La exposición a la radiación mamaria también se reduce sustancialmente con la exploración VQ en comparación con la CTPA y, por lo tanto, debe considerarse como una investigación de primera línea para la EP en mujeres en edad reproductiva. Se puede utilizar una exploración VQ normal para excluir la EP, mientras que una exploración de alta probabilidad justifica la anticoagulación. Todos los demás resultados sonasociado con una probabilidad intermedia de EP (10-40%) y, por lo tanto, se requieren más imágenes, normalmente CTPA.
La ecografía de las extremidades inferiores se puede utilizar como una investigación inicial, especialmente cuando hay síntomas concurrentes que sugieren TVP. El hallazgo de TVP justifica el comienzo de la anticoagulación, aunque aún se requiere una mayor investigación si no se encuentra evidencia de TVP. Esta estrategia es útil cuando existen preocupaciones con respecto a la exposición a la radiación, como durante el embarazo.
Limitaciones de los algoritmos de diagnóstico en el ámbito de la atención primaria
La mayoría de los estudios que evalúan los algoritmos de diagnóstico de la EP se han realizado en el ámbito del servicio de urgencias. La puntuación de Wells requiere que el médico emita un juicio con respecto a la probabilidad de EP en comparación con explicaciones alternativas, que en la mayoría de los estudios se guiaron no solo por los síntomas y signos clínicos, sino también por las investigaciones iniciales, como la radiografía de tórax y el electrocardiograma. Por lo tanto, se debe tener precaución al aplicar algoritmos de diagnóstico para la EP cuando el paciente se evalúa únicamente en el entorno de atención primaria, y se recomienda una evaluación inmediata de dichos pacientes en un departamento de emergencias, particularmente en aquellos con una alta probabilidad previa a la prueba.
Tabla 2. Puntaje de Wells
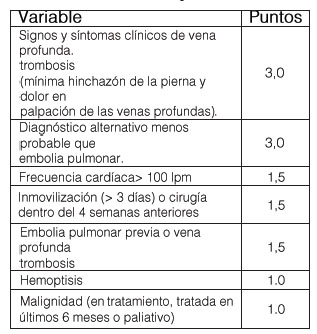
Fuente: (Wells, Anderson, & Rodger, 2000).
Tratamiento
La anticoagulación ha sido el pilar del tratamiento para la EP desde el estudio de (Barritt & Jordan, 1960) en el que el 25% de los pacientes que recibieron placebo murieron de EP recurrente, y todos los pacientes tratados con terapia anticoagulante sobrevivieron.
Elección del anticoagulante inicial
Debido al retraso en el efecto terapéutico de la Warfarina, es necesario el tratamiento inicial con un anticoagulante parenteral en pacientes con EP aguda. Se ha descubierto que la HBPM subcutánea basada en el peso es al menos tan eficaz y segura como la heparina intravenosa no fraccionada en el tratamiento de la EPy tiene el beneficio adicional de no requerir monitorización terapéutica, por lo que se puede administrar a una dosis fija basada en el peso. Por tanto, la heparina de bajo peso molecular suele ser el agente de elección para el tratamiento inicial de la EP. La heparina no fraccionada se sigue prefiriendo en pacientes con insuficiencia renal significativa, debido al aclaramiento renal de HBPM, y también se recomienda en pacientes inestables en los que aún se puede considerar la terapia trombolítica.
Tratamiento hospitalario versus ambulatorio
La capacidad de administrar HBPM por vía subcutánea ha significado que ahora teóricamente es posible la terapia ambulatoria de la EP. Hay datos de observación limitados que respaldan la seguridad de este enfoque en pacientes de bajo riesgo con EP (Janjua, Badshah, & Matta, 2015) Se han desarrollado herramientas para identificar un subgrupo de pacientes con EP de bajo riesgo potencialmente más adecuado para la terapia ambulatoria. Sin embargo, la seguridad de la terapia hospitalaria versus la terapia ambulatoria completa aún no se ha examinado en ensayos aleatorizados y, por lo tanto, todavía se recomienda un período corto de evaluación hospitalaria inicial para los pacientes con EP hasta que se realicen dichos ensayos.
Se acepta que la trombólisis está indicada en pacientes con EP que presentan inestabilidad hemodinámica (PA sistólica <90 mmHg), debido a una alta tasa de letalidad con la terapia anticoagulante estándar. Se ha propuesto que los pacientes sin compromiso hemodinámico con marcadores de mal pronóstico presentes, como dilatación del ventrículo derecho o troponina elevada, también deberían ser considerados para terapia trombolítica. Sin embargo, no existen estudios aleatorizados que demuestren claramente que la trombólisis temprana mejora la supervivencia en este subgrupo de pacientes con EP, siempre que se pueda administrar trombólisis de rescate en caso de deterioro clínico.
Duración de la anticoagulación
Después del período de tratamiento inicial con HBPM, la warfarina generalmente se usa para la anticoagulación continua, con un índice normalizado internacional (INR) objetivo recomendado de 2.0 a 3.0. Se recomienda un mínimo de 3 meses de anticoagulación en pacientes con EP sintomática, ya que el riesgo de trombosis recurrente aumenta en pacientes que reciben un tratamiento de menor duración.
El predictor más fuerte del riesgo de eventos recurrentes son las circunstancias en el momento del evento inicial. En pacientes con EP asociada con un factor de riesgo inductor definido, como una cirugía mayor reciente, el riesgo de recurrencia es generalmente bajo y es suficiente un tratamiento anticoagulante de 3 a 6 meses. En pacientes con PE no provocado el riesgo de recurrencia es mayor y puede estar indicada la anticoagulación a largo plazo. (Schreijer, Cannegieter, & Doggen, 2018)
Esto se aplica particularmente si hay factores de pronóstico adicionales que se sabe que están asociados con un mayor riesgo de recurrencia, incluido el sexo masculino, la antitrombina, la deficiencia de proteína C y proteína S o el síndrome de anticuerpos antifosfolípidos. La decisión sobre la duración de la anticoagulación en estos pacientes debe tomarse junto con un especialista interesado en la trombosis venosa.
Conclusión
La embolia pulmonar sigue siendo una enfermedad potencialmente mortal por la que se debe mantener una alta sospecha diagnóstica. Es probable que en el futuro se mejoren las estrategias para la estratificación del riesgo de los pacientes con EP, identificando a los pacientes de bajo riesgo que puedan ser tratados como pacientes ambulatorios y a los pacientes de alto riesgo que probablemente se beneficien de una intervención más agresiva.
La aparición de nuevos anticoagulantes orales, como el inhibidor directo de la trombina dabigatrán y el inhibidor del factor Xa rivaroxabán,que tienen el potencial de usarse tanto para la anticoagulación inicial como para la anticoagulación a largo plazo sin necesidad de seguimiento terapéutico, es probable que simplifique el tratamiento de los pacientes con trombosis venosa. Sin embargo, el papel exacto de estos agentes aún no se ha determinado y se verá influido por el costo de los medicamentos, que a su vez influirá en las restricciones que se impongan a la disponibilidad de los medicamentos
REFERENCIAS BIBLIOGRÁFICAS
Barritt, D., & Jordan, S. (1960). Anticoagulant drugs in the treatment of pulmonary embolism: a controlled trial. Lancet , 1309–12.
Blom, J., Doggen, C., & Osanto, S. (2015). Neoplasias, mutaciones protrombóticas y riesgo de trombosis venosa. JAMA, 715–722.
Bolívar, J. (2015). Investigación Documental. México. Pax.
Cannegieter, S., Doggen, C., van Houwelingen, H., & Rosendaal, F. (2016). Travel-related venous thrombosis: results from a large population–based case control study (MEGA Study). PLoS Med, 307.
Castro, J. (2016). Técnicas Documentales. México. Limusa.
Chuang, Y., & Yu, C. (2016). Clinical characteristics and outcomes of lung cancer with pulmonary embolism. Oncology, 100–106.
Chunilal, S., Eikelboom, J., & Attia, J. (2013). Does this patient have pulmonary embolism. JAMA, 2849–58.
Davila, A. (2015). Diccionario de Términos Científicos. . Caracas: Editorial Oasis.
Heit, J. (2015). Venous thromboembolism: disease burden, outcomes and risk factors. J Thromb Haemost, 1611–7.
Hurwitz, L., Reiman, R., & Yoshizumi, T. (2017). Radiation dose from contem-porary cardiothoracic multidetector CT protocols with an anthropomorphic female phantom: implications for cancer induction. Radiology, 742– 50.
Janjua, M., Badshah, A., & Matta, F. (2015). Treatment of acute pulmonary embolism as outpatients or following early discharge – a systematic review. Thromb Haemost , 756–61.
Key, N., Khorana, A., & Kuderer, N. (2020). Venous thromboembolism prophylaxis and treatment in patients with cancer: ASCO clinical practice guideline update. J Clin Oncol, 496-520.
Kucher, N., Rossi, E., De Rosa, M., & Goldhaber, S. (2016). Massive pulmonary embolism. Circulation, 577–82.
Lee, A. (2014). Management of thrombosis in cancer: primary prevention and sec-ondary prophylaxis. Br J Haem, 291–302.
Li, Y. S., Wang, W., Ning, S., & Chen, H. (2018). Lung cancer and pulmonary embolism: what is the relationship? A review. J Cancer, 3046–3057.
Lidegaard, O., Løkkegaard, E., Svendsen, A., & Agger, C. (2016). Hormonal contracep-tion and risk of venous thromboembolism: national follow-up study. BMJ, 339.
Malgor, R., Bilfinger, T., & Labropoulos, N. (2012). Una revisión sistemática de la embolia pulmonar en pacientes con cáncer de pulmón. Ann Thorac Surg, 311–316.
Perrier, A., Roy, P., & Sanchez, O. (2015). Multidetector-row computed tomography in suspected pulmonary embolism. N Engl J Med, 1760–8.
Schreijer, A., Cannegieter, S., & Doggen, C. (2018). The effect of flight related behavior on the risk of venous thrombosis after air travel. Br J Haem, 425–42.
Simpson, E., Lawrenson, R., & Nightingale, A. (2011). Venous thromboem-bolism in pregnancy and the puerperium: incidence and additional risk factors from a London perinatal database. BJOG, 56–60.
Stein, P., & Henry, J. (2007). Clinical characteristics of patients with acute pulmo-nary embolism stratified according to their presenting syndromes. Chest, 974–9.
Stein, P., Willis, P., & De Mets, D. (1981). History and physical examination in acute pulmonary embolism in patients without preexisting cardiac or pulmonary disease. Am J Cardiol, 218–23.
Wells, P., Anderson, D., & Rodger, M. (2000). Derivación de un modelo clínico simple para categorizar la probabilidad de embolia pulmonar de los pacientes: aumento de la utilidad del modelo con el dímero D SimpliRED. Thromb Haemost, 416–20.
White, R. (2013). La epidemiología del tromboembolismo venoso. Circulation, 14–8.